بیماری دیستروفی عضلانی دوشن (DMD)[1]
دیستروفی عضلانی دوشن (DMD) یک بیماری شدید، پیشرونده و در نهایت کشنده است. متاسفانه این بیماری نه تنها یکی از شدیدترین اشکال دیستروفی عضلانی ارثی است، بلکه شایع ترین بیماری عصبی عضلانی ارثی است. بیماری DMD نسبت به سایر انواع، مانند دیستروفی عضلانی بکر[2](BMD)، با شدت بیشتری پیشرفت کرده و ویژگیهای خاص خود را دارد. این بیماری بهطور متوسط از هر 3500 تولد مرد، در یک مورد مشاهده میشود. بر اساس این آمار و با توجه به جمعیت 85 میلیونی ایران و در نظر گرفتن اینکه حدوداً نیمی از جمعیت را مردان تشکیل میدهند، احتمال میرود حدود 714/12 نفر در کشور به این بیماری مبتلا باشند.
علائم بیماری DMD
این بیماری معمولاً در کودکان ۳ تا ۶ ساله ظاهر میشود. کودکان ممکن است با مشکلاتی مانند دشواری در راه رفتن یا بلند شدن از حالت نشسته یا دراز کشیده مواجه شوند. والدین نیز ممکن است نشانههایی مانند ضعف عضلات در ناحیه شانه و لگن، خستگی غیرعادی و افتادنهای مکرر کودک را مشاهده کنند.
برخی از علائم و نشانههای دیگر این بیماری عبارتند از:
- ضعف و آتروفی تدریجی عضلات که معمولاً ابتدا در عضلات پاها و لگن ظاهر شده و سپس با شدت کمتر به بازوها، گردن و دیگر نواحی بدن گسترش مییابد.
- بزرگ شدن غیرطبیعی عضلات ساق پا (هیپرتروفی)
- مشکل در بالا رفتن از پلهها
- ناتوانی در پریدن
- راه رفتن روی پنجه پا
- درد در ناحیه پا
- ضعف عضلات صورت که میتواند مشکلاتی مانند ناتوانی در سوت زدن یا بستن کامل چشمها ایجاد کند.
علاوه بر موارد فوق، علائم دیگری نیز ممکن است وجود داشته باشد، از جمله:
- مشکلات قلبی، مانند ضربان نامنظم قلب یا بزرگ شدن عضله قلب
- دشواریهای تنفسی و تنگی نفس که معمولاً به دلیل انحنای ستون فقرات (اسکولیوز) به وجود میآید.
- کوتاهی قامت
- اختلالات شناختی و دشواریهای یادگیری
- تأخیر در رشد گفتار و زبان
علت ایجاد بیماری DMD
علت اصلی این بیماری، نقص ژنتیکی در کروموزوم X است که منجر به کمبود یا عدم وجود پروتئین دیستروفین میشود. به بیان دقیقتر، این شرایط ناشی از وجود نقص در یکی از ژنهای کروموزوم X، به نام ژن DMD است که وظیفه تولید پروتئین دیستروفین را برعهده دارد. جهش های ژنتیکی که باعث DMD می شوند، از تولید پروتئین دیستروفین که برای ثبات ماهیچه ضروری است، جلوگیری می کند. محصول ژن دیستروفین فیبرهای عضلانی را به غشای اطراف خود متصل می کند. بدون دیستروفین، عضلات در اثر استفاده عادی آسیب می بینند و منجر به ضعف می شوند.
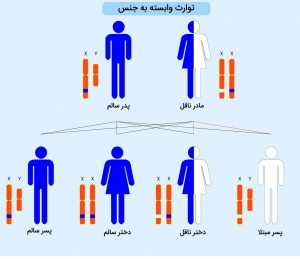
نحوه انتقال و وراثت بیماری DMD
DMD به عنوان یک بیماری ژنتیکی وابسته به جنس مغلوب شناخته میشود. در دو سوم موارد، پسر مبتلا بیماری را از مادر خود به ارث میبرد، مادری که ناقل بوده و جهش در یکی از نسخههای کروموزوم X او وجود دارد. شایان ذکر است که زنان ممکن است حامل جهش دیستروفین باشند و هیچ علائمی را نشان ندهند، اما ممکن است بعداً به مشکلاتی مانند کاردیومیوپاتی مبتلا شوند. جهش های مسبب بیماری DMD همچنین می تواند به عنوان یک تغییر خود به خود و به صورت غیرارثی در کودک ظاهر شود.
روشهای درمان بیماری DMD
برای سالهای زیادی، هیچ روش درمانی موثری برای این بیماری وجود نداشت. با این حال، امروزه گزینههای متعددی نظیر فیزیوتراپی، کاردرمانی، سلولدرمانی و ژندرمانی برای بهبود شرایط بیماران مبتلا به دیستروفی عضلانی دوشن فراهم شده است.
روش های تشخیص بیماری DMD
پزشکان معمولاً آزمایش خون کراتین کیناز [3](CK) را برای بررسی آسیب عضلانی قبل از انجام آزمایش ژنتیکی در صورت مشکوک بودن به DMD انجام می دهند. سطوح بالای CK نشاندهنده DMD احتمالی است و به دنبال آن آزمایش ژنتیکی از نمونههای خون یا بزاق و گاهی اوقات در صورت لزوم بیوپسی عضلانی انجام میشود. همچنین با توجه به اینکه بیماری DMD تقریباً همیشه بر عملکرد قلب تأثیرگذار است، پزشک معمولاً برای بررسی علائم و ارزیابی وضعیت سلامت قلب کودک، تست نوار قلب را توصیه می کند. آزمایش ژنتیک با شناسایی جهشهای خاص در ژن دیستروفین که از تولید عملکردی دیستروفین جلوگیری میکند، DMD را تأیید میکند. این آزمایش، DMD را از سایر دیستروفی های عضلانی با علائم مشابه متمایز می کند و شدت و پیشرفت بیماری را پیش بینی می کند. نکته جالب اینکه افراد مبتلا به DMD فاقد دیستروفین عملکردی هستند در حالی که مبتلایان به BMD دیستروفین محدودی دارند.
مروری بر انواع آزمایش های ژنتیکی برای بیماری DMD
آزمایش ژنتیک روش استاندارد برای تشخیص است. هنگامی که جهش DMD در کودک شناسایی شد، اعضای خانواده می توانند برای جهش آزمایش شوند. همچنین مادران و بستگان می توانند از طریق آزمایش ژنتیکی که می تواند برای تشخیص قبل از تولد نیز مورد استفاده قرار گیرد، در مورد خطر انتقال بیماری مطلع شوند.
آزمایش ژنتیک برای تشخیص DMDو انتخاب روش های درمانی مهم است. مشاوران ژنتیک به خانواده ها در درک نتایج آزمایش DMD کمک می کنند. آزمایش ژنتیک تأیید می کند که آیا مشکلات عضلانی ناشی از جهش در ژن دیستروفین است یا نه؟ این مورد برای تشخیص بیماری و درمان آن ضروری است. برای کودکانی که علائم DMD را نشان می دهند، اگر جهش DMD در کودک تایید شود، یک مشاور ژنتیک می تواند آزمایش را برای سایر اعضای خانواده پیشنهاد دهد. اقوام زن نیز باید مورد آزمایش قرار گیرند، و منفی بودن آزمایش مادر به دلیل احتمال موزائیسم رده زایا وضعیت ناقل را رد نمی کند.
با توجه به اندازه بزرگ ژن DMD ، نرخ جهش برای این ژن بسیار بالا است، به طوری که حدود یک سوم جهش ها به صورت جهش های جدید (de novo) اتفاق می افتد و مابقی ناشی از موزائیسم رده زایا یا به ارث بردن از یک مادر ناقل است. بیش از 7000 جهش مختلف دیستروفین در بیماران مبتلا به DMD یا BMD شناسایی شده است. تقریباً 60 درصد از جهشها در بیماران مبتلا به DMD حذفها و 11 درصد موارد مضاعف شدگی هستند و بقیه جهشهای کوچکی هستند که روی توالی کدکننده و نقاط ویرایش mRNA تاثیر میگذارند. حذف ها و تکرارها عمدتاً در دو نقطه داغ ژن DMD، واقع در اگزون های 3-9 و 45-55 رخ می دهد. در مرحله نخست، جهشهای حذف و مضاعف شدگی با استفاده از آزمایش MLPA بررسی میشوند و در صورت منفی بودن نتیجه، روش توالییابی اگزوم (WES) برای شناسایی جهشهای نقطهای به کار گرفته میشود. به کمک این دو روش، شناسایی تغییرات ژنتیکی مسئول بیماری در بیش از 95 درصد بیماران امکانپذیر است. در برخی موارد، بیوپسی عضله ممکن است برای بررسی بیشتر انجام شود.
بهترین زمان برای انجام بررسیهای ژنتیکی بیماری DMD پیش از بارداری است. این زمانبندی فرصت کافی را برای بررسی وضعیت ژنتیکی فرد و تعیین ناقل بودن او فراهم میکند. در صورتی که بتوان زنان ناقل را به موقع شناسایی کرد، میتوان با استفاده از آزمایشهای تشخیص پیش از تولد [4](PND) و آزمایش تشخیص ژنتیکی قبل از لانه گزینی [5](PGD) از تولد نوزادان مبتلا پیشگیری نمود.
آزمایش ژنتیکی پیش از تولد قادر است در صورت شناسایی جهش خاصی در خانواده، بیماری DMD را تشخیص دهد. ابتدا باید جهشای که در مادر ناقل وجود دارد، شناسایی شود. با توجه به پیچیدگی و زمانبر بودن بررسی جهشهای ژن DMD، بهتر است این فرآیند قبل از بارداری انجام شود. پس از این مرحله، وضعیت جنین از نظر وجود جهش میتواند با استفاده از آزمایش CVS یا آمنیوسنتز در هفتههای یازدهم تا پانزدهم بارداری بررسی شود، که معمولاً آزمایش [6]CVS ارجحیت دارد. اگر جهش در جنین شناسایی گردد، امکان بهکارگیری روشهای سقط درمانی برای جلوگیری از تولد نوزاد مبتلا وجود خواهد داشت. لازم به ذکر است که در ایران مهلت قانونی برای سقط درمانی تا پایان هفته هجدهم بارداری (هجده هفته و شش روز) تعیین شده است و نتایج آزمایشها باید پیش از این بازه زمانی آماده شود.
زوجهایی که خطر داشتن فرزند مبتلا به DMD در آنها وجود دارد، ممکن است روش PGD را در چهارچوب لقاح آزمایشگاهی [7](IVF)مد نظر قرار دهند. این روش شامل بررسی جنینها جهت انتخاب نمونههای سالم و فاقد جهش ژنی مرتبط با DMD است. جنینهای سالم شناساییشده سپس در رحم مادر قرار میگیرند. استفاده از این روش به پیشگیری از عوارض ناشی از سقط درمانی، چه روانی و چه جسمی، کمک شایانی میکند. از آنجا که بیماری DMD بیشتر در جنس مذکر ظاهر شده و به ندرت در دختران مشاهده میشود، انتخاب جنسیت دختر در روشهای کمک باروری میتواند به عنوان یکی از راههای پیشگیری از بروز این بیماری در خانواده مورد استفاده قرار گیرد.
آزمایشگاه پاتوبیولوژی و ژنتیک پزشکی بوعلی قم برای کمک به خانواده ها، یک خدمت جامع شامل انواع آزمایش های لازم و مرتبط با بیماری DMD و BMD را ارائه می دهد.
[1] Duchenne muscular dystrophy
[2] Becker muscular dystrophy
[3] Creatine kinase
[4] Prenatal Diagnosis
[5] Preimplantation Genetic Diagnosis
[6] Chorionic Villus Sampling
[7] In Vitro Fertilization
reference:
https://www.ncbi.nlm.nih.gov/books/NBK482346/
https://www.frontiersin.org/journals/physiology/articles/10.3389/fphys.2023.1183101/full
https://mytomorrows.com/blog/patients/duchenne-muscular-dystrophy-and-genetic testing/

